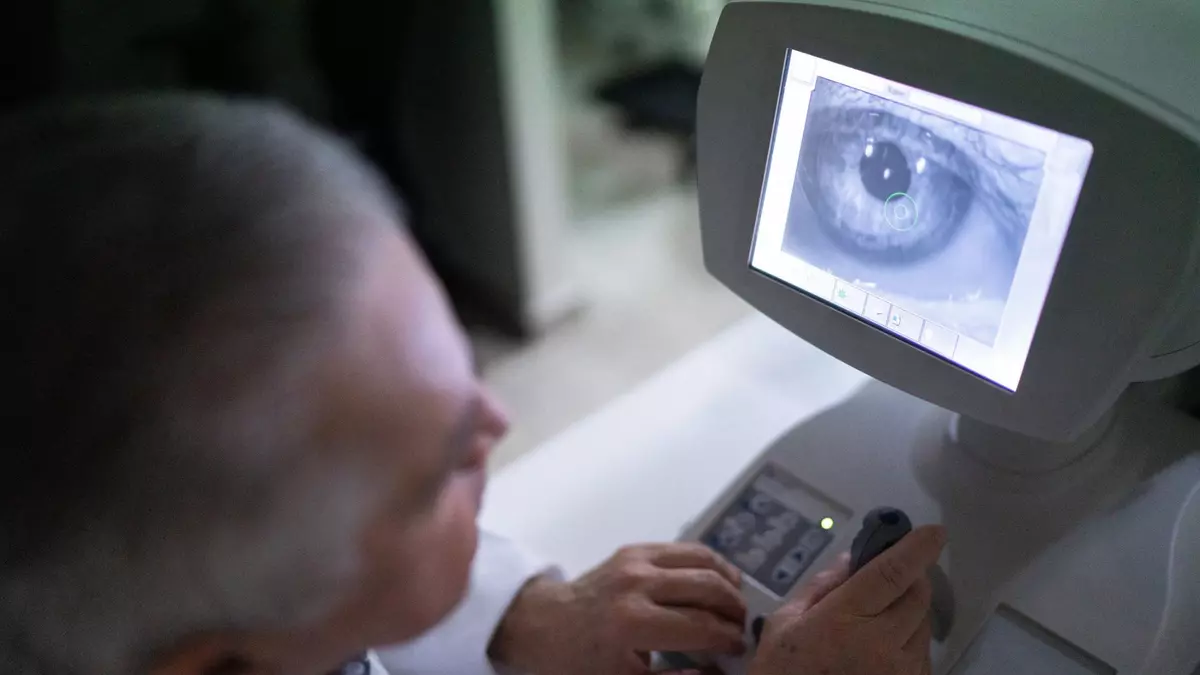
O glaucoma, uma doença ocular que gradualmente causa cegueira ao danificar o nervo óptico, geralmente é desencadeado pelo excesso de pressão do fluido no olho – mas algumas pessoas ainda perdem a visão mesmo depois que a pressão é aliviada.
Agora, uma nova pesquisa aponta para uma razão surpreendente: um grupo de células imunes do intestino pode ganhar a capacidade de se infiltrar na retina, o tecido sensível à luz na parte de trás do olho, causando estragos.
Essas células – combatentes de doenças conhecidas como “células T auxiliares” que carregam uma proteína chamada beta 7 – normalmente não têm a capacidade de atravessar o nervo óptico até o olho, mas algo nos estágios iniciais do glaucoma parece desencadear um padrão de ativação bizarro que acaba alterando as células T e piorando a progressão da doença.
“Em nosso estudo, observamos que a ‘educação intestinal’ potencialmente leva a uma reprogramação fundamental das células T no sangue periférico de camundongos com glaucoma”, disse um dos líderes do estudo, Fang Lu, pesquisador da Academia de Ciências Médicas de Sichuan e do Sichuan’s People’s People’s Hospital na China.
Estudos anteriores mostraram que, tanto em camundongos quanto em humanos, o glaucoma é marcado por uma infiltração de células T na retina. Quando essas células T específicas são transferidas para a retina de um camundongo saudável, elas causam danos semelhantes aos do glaucoma. Os pesquisadores do estudo também descobriram anteriormente que essas células T expressam um receptor que permite que elas viajem do intestino para a retina. Uma vez no olho, essas células “licenciadas pelo intestino” podem se agarrar a uma molécula no revestimento da retina para passar para o tecido.
“Com base nessas descobertas, levantamos a hipótese de que pode haver uma conexão entre as células T expostas ao intestino, sua migração para a retina e a progressão do glaucoma”, disse Lu.
No novo estudo, publicado na revista Science Translational Medicine quarta-feira (2), a equipe descobriu que pessoas com glaucoma têm níveis elevados dessas células T licenciadas pelo intestino no sangue. Eles descobriram isso analisando o sangue de quase 520 pacientes com glaucoma e cerca de 190 pacientes sem glaucoma. Quanto maior o nível de células licenciadas pelo intestino na corrente sanguínea de uma pessoa, maior o dano causado pelo glaucoma.
Usando um modelo de glaucoma em camundongos, a equipe revelou que essas células usam suas licenças para visitar o intestino, onde são geneticamente “reprogramadas” para ativar genes diferentes do normal. As células então correm para a retina, onde contribuem diretamente para o dano. É a reprogramação que dá às células o que Lu chamou de “uma capacidade notável de atingir a retina”.
Os pesquisadores identificaram uma proteína dentro da retina à qual as células T expostas ao intestino podem se ligar, permitindo que elas entrem no tecido ocular; as células T normais não podem se prender a essa proteína. Quando os pesquisadores bloquearam essa proteína e a interação das células T, eles observaram significativamente menos dano ao glaucoma.
Os pesquisadores ainda não têm certeza do que faz com que essas células T se descontrolem. Mas eles descobriram que, quando as células T são expostas à pressão ocular elevada, elas migram para o intestino em camundongos. Assim, o estresse local do aumento da pressão ocular pode desencadear uma espiral inflamatória no corpo, que empurra as células T para um padrão de ativação perigoso.
No entanto, exatamente o que acontece no intestino para reprogramar essas células permanece uma questão em aberto, disse Lu.
Se os mecanismos descobertos no estudo com camundongos forem verdadeiros para humanos, isso pode abrir novos caminhos para o tratamento do glaucoma, disse Lu. A equipe descobriu que o vedolizumab, um medicamento que trata a doença inflamatória intestinal, preveniu danos à retina em camundongos com aumento da pressão ocular. Mais pesquisas e estudos clínicos serão necessários para ver se esse tratamento é promissor para pacientes com glaucoma.
“Nossos próximos passos envolvem aprofundar o papel do ambiente intestinal na modulação das células T”, disse Lu.